Δρ Δημήτριος Ν. Γκέλης (MD, ORL, DDS, PhD)
| Η χρόνια ρινοκολπίτιδα μπορεί να συνυπάρχει με ή χωρίς ρινικούς πολύποδες. Μερικά άτομα με χρόνια ρινοκολπίτιδα με ρινικούς πολύποδες [ CRSwNP] δεν ανταποκρίνονται στην καθιερωμένη τυπική φαρμακευτική και χειρουργική θεραπεία. Για αυτά τα άτομα, τα βιολογικά φάρμακα εμφανίζονται ως μια σημαντική θεραπευτική εναλλακτική λύση. Μέχρι τώρα έχουν γίνει μελέτες βιολογικών φαρμάκων (μονοκλωνικά αντισώματα) που αφορούν τη χρήση αντι-ΙgE ανοσοσφαιρίνης Ε (omalizumab), αντι-ιντερλευκίνης 5 (mepolizumab και reslizumab) και αντι-ιντερλευκίνης 4 / ιντερλευκίνης 13 (dupilumab, benralizumab και tezepelumab) και της μικκυλιακής κουρκουμίνης (Curcugkel) |
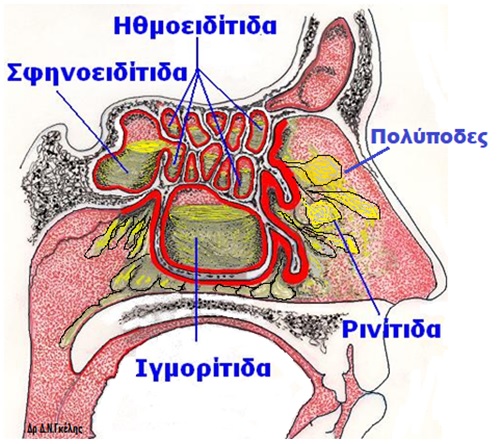 Οι δυσίατες μορφές χρόνιας ρινοκολπίτιδας, οι οποίες είναι ανθεκτικές στη συμβατική φαρμακευτική ή χειρουργική θεραπεία σήμερα αντιμετωπίζονται με σημαντικού βαθμού επιτυχία με τη χορήγηση κάποιου από τα εγκεκριμένα βιολογικά φάρμακα[1].
Οι δυσίατες μορφές χρόνιας ρινοκολπίτιδας, οι οποίες είναι ανθεκτικές στη συμβατική φαρμακευτική ή χειρουργική θεραπεία σήμερα αντιμετωπίζονται με σημαντικού βαθμού επιτυχία με τη χορήγηση κάποιου από τα εγκεκριμένα βιολογικά φάρμακα[1].
Τα διαθέσιμα σήμερα βιολογικά φάρμακα έχουν τύχει εκτεταμένων κλινικών ερευνών, πράγμα που διευκολύνει την ασφαλή συνταγογράφησή τους από τους ωτορινολαρυγγολόγους.
Σήμερα, τα βιολογικά φάρμακα που αρχικά εφαρμόστηκαν στη θεραπεία του δυσίατου άσθματος χρησιμοποιούνται και για τη θεραπεία της χρόνιας ρινοκολπίτιδας με ρινικούς πολύποδες (CRSwN), που μπορεί να συνυπάρχουν ή να μη συνυπάρχουν με άσθμα. Η θεραπεία της χρόνιας ρινοκολπίτιδας με πολύποδες με κάποιο βιολογικό φάρμακο στηρίζεται στην αποκλειστική δράση του βιολογικού φαρμάκου κατά της φλεγμονής τύπου 2, που αποτελεί το παθολογοανατομικό υπέδαφος της νόσου.
Η φλεγμονή τύπου 2, που παλαιότερα ονομαζόταν φλεγμονή βοηθητικού κυττάρου Τ τύπου 2 (Th2), ενορχηστρώνεται από φλεγμονώδεις χημικούς μεσολαβητές, που παράγονται από κύτταρα Th2, όπως οι κυτοκίνες IL-4, IL-5, IL-9 και IL-13. Αυτές οι κυτοκίνες έχουν τα ηωσινόφιλα ως τον κύριο κυτταρικό δείκτη τους, εκτός από την υψηλή παρουσία τοπικής ή κυκλοφορούσας IgE, την οποία παράγουν.
Με την επακόλουθη αναγνώριση της συμμετοχής στη χρονιότητα της φλεγμονής και άλλων μη-Th2 κυττάρων ικανών να παράγουν το ίδιο προφίλ κυτοκίνης, όπως τα έμφυτα λεμφοειδή κύτταρα τύπου 2 (ILC2), η φλεγμονή έγινε γνωστή ως τύπου 2.
Η κλινική έρευνα έχει αναγνωρίσει ότι η χρόνια ρινοκολπίτιδα περιλαμβάνει μια σειρά μορφών ή καταστάσεων με διαφορετικές παθοφυσιολογικές βάσεις, αν και έχουν κοινά κλινικά χαρακτηριστικά. Κατά συνέπεια, συγκεκριμένες μορφές χρόνιας ρινοκολπίτιδας έχουν διαφορετική πρόγνωση και ανταποκρίσεις σε μια δεδομένη θεραπεία. Μια πρόσφατη πολυκεντρική μελέτη αποκάλυψε ότι το 35% των ασθενών με CRSwNP είχαν υποτροπή εντός 6 μηνών[2].
Στην προσπάθεια εντοπισμού των παραγόντων που πιθανώς σχετίζονται με επιδείνωση των αποτελεσμάτων, ο ενδοτυπισμός, μέσω της χρήσης βιοδεικτών, μπορεί να βοηθήσει στον εντοπισμό των ασθενών με φλεγμονή τύπου 2 και ο οποίος θα ανταποκρινόταν καλύτερα σε αυτές τις νέες θεραπείες[3].
Η χρόνια ρινοκολπίτιδα μπορεί να συνυπάρχει με ή χωρίς ρινικούς πολύποδες, καθώς και με ή χωρίς βρογχικό άσθμα. Η χρόνια ρινοκολπίτιδα με ρινικούς πολύποδες (CRSwNP) είναι μια από τις πιο σοβαρές μορφές χρόνιας ρινοκολπίτιδας. Η CRSwNP χαρακτηρίζεται από ρινική συμφόρηση, δυσχέρεια ρινικής αναπνοής, απώλεια της όσφρησης, διαρκή μόνιμη ρινόρροια και οπισθορρινικό κατάρρου.
Οι μέχρι πρόσφατα εφαρμοζόμενες θεραπείες ήταν αναποτελεσματικές, όσον αφορά στον έλεγχο της υποτροπής της νόσου, παρά τους πολλαπλούς κύκλους ιατρικών και χειρουργικών θεραπειών. Η από του στόματος θεραπεία με κορτικοστεροειδή και με ψεκασμούς υπέρτονου φυσιολογικού ορού χρησιμοποιούνται συχνά για τον έλεγχο των παροξύνσεων, που αφήνουν όμως τον ασθενή εκτεθειμένο σε ανεπιθύμητες ενέργειες που προκαλούνται από τα κορτικοστεροειδή. Έτσι, υπήρξε μια σαφής ανάγκη για νέες θεραπείες για την επίτευξη καλύτερου ελέγχου της νόσου. Βεβαίως η χειρουργική θεραπεία με λειτουργική ενδοσκοπική χειρουργική επέμβαση (FESS), ,παρα τη ριζικότητά της δεν εξασφαλίζει πάντοτε τους ασθενείς ότι δεν θα υποτροπιάσει η νόσος, αφού δεν έχει ανατραπεί ο παθοφυσιολογικός μηχανισμός που τη δημιούργησε και τη συντηρεί[4].
Τα αποτελέσματα της δράσης των από του στόματος χορηγούμενων αντιβιοτικών στη χρόνια ρινοκολπίτιδα με ή χωρίς ρινικούς πολύποδες είναι η αύξηση της συχνότητας της αντοχής των βακτηριδίων στα αντιβιοτικά, η έκταση της οποίας δεν έχει ακόμη πλήρως αξιολογηθεί, αλλά μπορεί να είναι σημαντική, ενώ έχει εμφανιστεί επίσης αντοχή και στα κορτικοστεροειδή.
Η χρόνια ρινοκολπίτιδα με ρινικούς πολύποδες (CRSwNP), που επιπλέκεται με άσθμα θεωρείται πιο σοβαρή κατάσταση και μπορεί να έχει σημαντικό αντίκτυπο στην ποιότητα της ζωής του ασθενούς ή ακόμη και σ΄αυτή την ίδια τη ζωή των ασθενών, καθ΄όσον ο αριθμός των ατόμων με άσθμα, που χάνει τη ζωή τους παραμένει σταθερός τα τελευταία χρόνια.
Bεβαίως η νοσηρότητα και η θνησιμότητα του άσθματος έχουν βελτιωθεί σημαντικά τα τελευταία 15 χρόνια και οι περισσότεροι ασθενείς μπορούν να επιτύχουν καλό έλεγχο του άσθματος. Ωστόσο, η υποθεραπεία των ασθματικών ασθενών εξακολουθεί να είναι συνήθης. Γιαυτό απαιτείται εκπαίδευση των ασθενών και λεπτομερής ενημέρωσή τους για την αποτελεσματικότητα των συγχρόνων θεραπειών του άσθματος και των ρινικών πολυπόδων. Η διαχείριση των ασθενών με άσθμα και ρινικούς πολύποδες αποτελείται από έναν κύκλο αξιολόγησης του ελέγχου του άσθματος και των πολυπόδων και των παραγόντων κινδύνου και προσαρμογής των φαρμάκων, ανάλογα με τον κάθε ασθενή.
Το μέτριο ή σοβαρό άσθμα είναι μια σύνθετη διαδικασία ασθένειας που εκδηλώνεται κλινικά ως τουλάχιστον μερικώς αναστρέψιμη απόφραξη των αεραγωγών λόγω υπερανταπόκρισης των αεραγωγών. Η θεραπεία του άσθματος βασιζόταν κυρίως στον έλεγχο των συμπτωμάτων, έως ότου πρόσφατες μελέτες των μηχανισμών της οδήγησαν σε μια σειρά από νέες στοχευμένες, ασφαλείς και αποτελεσματικές θεραπείες, τις λεγόμενες βιολογικές. Αυτές οι βιολογικές θεραπείες επιτίθενται άμεσα στους ένοχους φλεγμονώδεις μεσολαβητές σε μοριακό επίπεδο[5].
Με την εισαγωγή στη θεραπευτική των βιολογικών θεραπειών, η διαχείριση του σοβαρού άσθματος έχει εισέλθει στην εποχή της ιατρικής ακριβείας – μια στροφή που οδηγεί τις κλινικές φιλοδοξίες προς την ύφεση της νόσου. Οι ασθενείς με σοβαρό άσθμα έχουν συχνά συνυπάρχουσες καταστάσεις που συμβάλλουν στα συμπτώματά τους, επιβάλλοντας μια πολυδιάστατη προσέγγιση διαχείρισης[6].
Τα βιολογικά φάρμακα, τα οποία στοχεύουν στη μείωση της φλεγμονής Τ2 και αποτελούν νέα θεραπευτική επιλογή για τους ασθενείς με δυσίατη ρινοκολπίτιδα με πολύποδες (CRSwNP).
Για τα άτομα με CRSwNP, η χρησιμοποίηση των βιολογικών φαρμάκων εμφανίζεται ως μια σημαντική θεραπευτική εναλλακτική λύση. Όμως πριν από τη χορήγηση οποιουδήποτε βιολογικού παράγοντα απαιτείται προσεκτική εξέταση πολλών παραγόντων, συμπεριλαμβανομένης της σοβαρότητας της νόσου, του κινδύνου υποτροπής των πολύποδων με ιατρική ή χειρουργική θεραπεία, οι προτιμήσεις και οι στόχοι των ασθενών, η ασφάλεια των ασθενών και τη σχέση κόστους-αποτελεσματικότητας.
Προς το παρόν υπάρχουν κλινικές μελέτες αποτελεσματικότητας της αντι-ΙgE ανοσοσφαιρίνης Ε (omalizumab), αντι-ιντερλευκίνης 5 (mepolizumab και rezlisumab) και αντι-ιντερλευκίνης 4 / ιντερλευκίνης 13 (dupilumab, benralizumab και tezepelumab). Αυτοί οι βιολογικοί παράγοντες έχουν δοκιμαστεί σε ασθενείς με χρόνια ρινοκολπίτιδα με ή χωρίς πολύποδες και με ή χωρίς άσθμα [7], καθώς και σε ασθενείς με σοβαρό άσθμα. Eπίσης προστέθηκαν στο omalizumab, που πρώτο χρησιμοποιήθηκε σε ασθενείς με στόχο την πρόληψη των υποτροπών και της επιδείνωσης του σοβαρού άσθματος και για τη μείωση της χρήσης των κορτικοστεροειδών και του περιορισμού των παρενεργειών τους[8].
Παθοφυσιολογικός μηχανισμός της πρόκλησης της χρόνιας ρινοκολπίτιδας με ρινικούς πολύποδες (CRSwNP)
Συνήθως η χρόνια ρινοκολπίτιδα αποδίδεται σε μια Th2 αντίδραση. Αν και τα κύτταρα Th2 παίζουν σημαντικό ρόλο στις αλλεργικές ασθένειες, η κύρια λειτουργία των κυττάρων Th2 πιστεύεται ότι είναι η παραγωγή κυτοκινών Th2, όπως η ιντερλευκίνη (IL) -4, IL-5, IL-13. Σήμερα είναι γνωστές πλέον οι νέες λειτουργίες των Th2 κυττάρων στις αλλεργικές ασθένειες.
Επιπλέον, έχουν βρεθεί νέοι μηχανισμοί παραγωγής ισταμίνης χρησιμοποιώντας in vitro καλλιέργειες μακροφάγων λευκοκυττάρων και Th2 κυττάρων.
Τόσο τα μακροφάγα όσο και τα κύτταρα Th2 παράγουν ισταμίνη μέσω της αλληλεπίδρασης μέ αντιγόνα. Αυτός είναι ένας νέος αλλεργικός μηχανισμός διαφορετικός από το μηχανισμό της δράσης της IgE επί των μαστοκυττάρων [9].
Γνωρίζοντας ποια ιντερλευκίνη συμμετέχει στην δημιουργία του άσθματος και των ρινικών πολυπόδων, σε κάθε ασθενή γίνεται εργαστηριακός έλεγχος και μετρώνται τα επίπεδα της ΙL-4, IL-5, IL-13, των ολικών IgE και βάσει αυτών των ευρημάτων αποφασίζεται ποιος βιολογικός παράγοντας θα χρησιμοποιηθεί στον κάθε ασθενή.
Θεραπεία της χρόνιας ρινοκολπίτιδα με ρινικούς πολύποδες (CRSwNP) με βιολογικά φάρμακα
Πρόσφατα, οι μελέτες βιολογικών φαρμάκων έχουν ανοίξει νέο δρόμο θεραπείας της νόσου της ανώτερης και κατώτερης αεροφόρας οδού και ειδικά της χρόνιας ρινοκολπίτιδας με ρινικούς πολύποδες (CRSwNP), που προκαλείται με Th2 αντίδραση. Αυτή η αντιμετώπιση ανοίγει μια νέα θεραπευτική προσέγγιση σε σύγκριση με την τυπική θεραπεία.
Η βιολογική θεραπεία μπορεί να βοηθήσει στη βελτίωση των ασθενών με δυσίατη ή ανθεκτική στη θεραπεία CRSwNP, να μειώσει το μέγεθος των πολυπόδων και να βελτιώσει την όσφρηση.
Στους βιολογικούς παράγοντες που χρησιμοποιούνται κατά της CRSwNP περιλαμβάνονται και τα μονοκλωνικά αντισώματα.
Tα μονοκλωνικά αντισώματα είναι άκρως ειδικά αντισώματα, που παράγονται σε μεγάλες ποσότητες από τους κλώνους ενός ενιαίου υβριδώματος κυττάρου. Τα υβριδικά κύτταρα κλωνοποιούνται και δημιουργούνται κυτταρικές σειρές που παράγουν ένα ειδικό αντίσωμα που είναι χημικώς και ανοσολογικά oμογενές.
Τα μονοκλωνικά αντισώματα, που χρησιμοποιούνται κυρίως για τη θεραπεία του άσθματος, έχει πρόσφατα αποδειχθεί ότι, έχουν θετική επίδραση στον έλεγχο των συμπτωμάτων της χρόνιας ρινοκολπίτιδας και στη μείωση της ανάγκης για ενδοσκοπική χειρουργική των παραρρίνιων κόλπων [10].
 Τα μονοκλωνικά αντισώματα που έχουν ερευνηθεί ή ακόμη ερευνώνται, επί του παρόντος, για τη θεραπεία της δυσίατης ή ανθεκτικής στην κλασσική θεραπεία χρόνιας ρινοκολπίτιδας με ή χωρίς πολύποδες είναi [Βλέπε Πίνακα παραπλεύρως}:
Τα μονοκλωνικά αντισώματα που έχουν ερευνηθεί ή ακόμη ερευνώνται, επί του παρόντος, για τη θεραπεία της δυσίατης ή ανθεκτικής στην κλασσική θεραπεία χρόνιας ρινοκολπίτιδας με ή χωρίς πολύποδες είναi [Βλέπε Πίνακα παραπλεύρως}:
Τα φάρμακα αυτά διατίθενται αποκλειστικά σε ασθενείς με επίμονο αλλεργικό άσθμα (τύπου 2) σταδίου 5 ή 6, οι οποίοι δεν ελέγχονται επαρκώς με τα εισπνεόμενα κορτικοστεροειδή υψηλής δόσης και θεραπεία με β αγωνιστή μακράς δράσης, σύμφωνα με τις κατευθυντήριες οδηγίες της Παγκόσμιας Πρωτοβουλίας για το Άσθμα. [11, 12, 13].
Η Αnti-IgE ανοσοσφαιρίνη [omalizumab, Xolair®] δρα δεσμεύοντας τους υποδοχείς της IgE και στη συνέχεια αποτρέποντας τη σύνδεση IgE σε μαστοκύτταρα, δενδριτικά κύτταρα και βασεόφιλα μέσω των υποδοχέων FcεR1 και FcεR2 [14, 15].
Το Anti-IgE δεν έχει αντίστροφο αποτέλεσμα στην ήδη δεσμευμένη IgE. Μια πιο λεπτομερής ανάλυση των ανοσολογικών μηχανισμών που διέπουν την παθογένεση του άσθματος δείχνει ότι η ιντερλευκίνη 5 (IL-5) είναι μια κρίσιμη κυτοκίνη σε διάφορους φαινοτύπους του άσθματος. Στην πραγματικότητα, η IL-5 ασκεί επιλεκτική δράση στα ηωσινόφιλα, τα οποία, με τη σειρά τους, διατηρούν τη φλεγμονή των αεραγωγών και επιδεινώνουν τα συμπτώματα και τον έλεγχο του άσθματος.
Οι κλινικές δοκιμές έδειξαν ότι τα φάρμακα που στοχεύουν την IL-5 ή την υπομονάδα υποδοχέα άλφα (IL-5Ra) είναι μια πολλά υποσχόμενη θεραπευτική προσέγγιση για το σοβαρό άσθμα.
Τα χαρακτηριστικά αυτών των φαρμάκων ελαχιστοποιούν την τυπική κλασσική θεραπεία, καθώς τα συστηματικά κορτικοστεροειδή ελέγχουν μόνο μερικώς την ασθένεια και η δράση τους συνοδεύεται και από τις γνωστές ανεπιθύμητες ενέργειες [16].
Η μπενραλιζουμάμπη [benralizumab (Fasenra®)] που έχει αντι-IL-5 και αντι-ILRa δράση είναι αντισώματα που λειτουργούν στοχεύοντας την IL-5.
Οι παράγοντες κατά της IL-5 συνδέονται και εξουδετερώνουν την IL-5, η οποία παρεμβαίνει στην σχέση της με την αντι-IL-5Ra, η οποία εκφράζεται στα ηωσινόφιλα.
Η Anti-IL-5 Ra στοχεύει άμεσα την αλυσίδα anti-IL-5 Ra και προκαλεί λύση του κυττάρου στόχου. Λόγω αυτού του μηχανισμού, οι αντι-IL-5 και αντι-IL-5 Ra παράγοντες είναι αποτελεσματικοί στη μείωση της περιφερικής ηωσινόφιλης έκφρασης.
Η ομαλιζουμάμπη ( Omalizumab, Xolair®) και η μεπολιζουμάμπη (mepolizumab, (Nucala®) φέρουν προειδοποιήσεις ότι μπορεί να έχουν ως ανεπιθύμητη ενέργεια την αναφυλαξία.
Τα κριτήρια επιλεξιμότητας ασθενών για την για αντι-IgE θεραπεία περιλαμβάνουν τα αυξημένα επίπεδα ολικής IgE (30 IU / mL≤1500IU / mL), παροξύνσεις του άσθματος εντός ενός έτους και η θετική δερματική δοκιμασία ή in vitro αντιδραστικότητα σε ένα ολοετήσιο αεροαλλεργιογόνο.
Τα κριτήρια επιλεξιμότητας ασθενών στους οποίους μπορεί γίνει αντι-IL-5 και αντι-IL-5 Rα αγωγή περιλαμβάνουν το βασικό επίπεδο περιφερειακών ηωσινοφίλων ≥150 κυττάρων / μL (≥400 κύτταρα / μL) για την ρεσλισουμάμπη ( reslizumab) εντός των προηγούμενων 6 εβδομάδων, ο ηωσινόφιλος φαινότυπος και οι παροξύνσεις μέσα σε ένα χρόνο [16].
Τα αποτελέσματα της κλινικής έρευνας στη θεραπεία της CRSwNP με omalizumab (Xolair)
Η χρόνια ρινοκολπίτιδα με ρινικούς πολύποδες (CRSwNP) χαρακτηρίζεται από υπερπαραγωγή IgE και ηωσινοφιλική φλεγμονή. Το αντίσωμα anti- Ig [omalizumab], έχει αποδείξει αποτελεσματικότητα σε ασθενείς με CRSwNP, που πάσχουν ταυτόχρονα με άσθμα.
Ig [omalizumab], έχει αποδείξει αποτελεσματικότητα σε ασθενείς με CRSwNP, που πάσχουν ταυτόχρονα με άσθμα.
Philippe Gevaert και οι συνεργάτες μελέτησαν την αποτελεσματικότητα του omalizumab και προσδιόρισαν την ασφάλειά του στην CRSwNP σε δύο κλινικές μελέτες φάσης 3 (POLYP 1 και POLYP 2). Και βρήκαν ότι η ομαλιζουμάμπη βελτίωσε σημαντικά τα ενδοσκοπικά, κλινικά και αναφερόμενα από τον ασθενή αποτελέσματα σε σοβαρή CRSwNP με ανεπαρκή ανταπόκριση στα ενδορινικά κορτικοστεροειδή και ήταν καλά ανεκτή.
Συνοπτικά με το Omalizumab (Xolair) ολοκληρώθηκαν 2 κλινικές μελέτες φάσης 3, POLYP I (n = 138) και POLYP II (n = 127), με πολλά υποσχόμενα αποτελέσματα. Τα άτομα τυχαιοποιήθηκαν και τους χορηγήθηκε υποδορίως omalizumab έναντι εικονικού φαρμάκου για 24 εβδομάδες. Η δόση του omalizumab βασίστηκε στο βάρος και τα επίπεδα IgE ορού. Και οι δύο δοκιμές έδειξαν σημαντική μέση βελτίωση στα συμπρωτεύοντα τελικά σημεία. Σε σύγκριση με το εικονικό φάρμακο για τη βαθμολογία ρινικού πολύποδα, η διαφορά του σκέλους θεραπείας ήταν −1,14 (95% CI: −1,59 έως −0,69) στον POLYP I και −0,59 (95% CI: −1,05 έως −0,12) στον POLYP II. Για τη βαθμολογία ρινικής συμφόρησης, η διαφορά του βραχίονα θεραπείας ήταν −0,55 (95% CI: −0,84 έως −0,25) στον POLYP I και −0,50 (95% CI: −0,80 έως −0,19) στον POLYP II. Η συνολική βαθμολογία ρινικών συμπτωμάτων (συμπεριλαμβανομένης της ρινικής συμφόρησης, της όσφρησης, της ρινικής καταρροής και του οπισθορρινικού κατάρρου), τα μεμονωμένα συμπτώματα όπως η αίσθηση της όσφρησης και η ποιότητα ζωής της συγκεκριμένης ασθένειας βελτιώθηκαν σημαντικά από την αρχική τιμή στην ομάδα του omalizumab σε σύγκριση με το εικονικό φάρμακο[17].
Το Omalizumab (Xolair, Genentech) είναι ένας ανοσοτροποποιητής που είναι εγκεκριμένος από τον FDA για τη θεραπεία του άσθματος. Ωστόσο, το omalizumab στοχεύει τα μαστοκύτταρα και τα βασεόφιλα, όχι τα ηωσινόφιλα που επιδεινώνουν τη φλεγμονή σε έναν ασθενή με ηωσινοφιλικό άσθμα. Συνεπώς, δεν θα πρέπει να θεωρείται ως θεραπευτική επιλογή για αυτούς τους ασθενείς[18].
Τα αποτελέσματα της κλινικής έρευνας στη θεραπεία της CRSwNP με ντουπιλουμάμπη [dupilumab, (Dupixent®), Sanofi και Regeneron)]
Ο ρόλος των ανοσολογικών αντιδράσεων τύπου 2 στη χρόνια ρινοκολπίτιδα, στη σοβαρότητα της νόσου και στην υποτροπή και τις συννοσηρότητές της είναι πλέον αποδεδειγμένος. Στην παθοφυσιολογία της χρόνιας ρινοκολπίτιδας με ή χωρίς πολύποδες και με συνύπαρξη ό όχι άσθματος συμμετέχουν οι ιντερλευκίνες IL-4, IL-5 , IL-13 καθώς και η IgE.
Οι ασθενείς με τις παραπάνω καταστάσεις μπορεί να αντιμετωπιστούν και με βιολογικά φάρμακα (biologics), που στοχεύουν τις IL-4, IL-5 και την IL-13 καθώς και IgE. Οι θεραπείες αυτές ξεκίνησαν σε ασθενείς στα πλαίσια μικρών μελετών αποδείξεων της ιδέας (proof-of-concept).
Η πρόοδος στην κατανόηση των φλεγμονωδών διεργασιών Τύπου 2 που συμβαίνουν στο 80% περίπου των ασθενών με CRSwNP του δυτικού κόσμου έχουν οδηγήσει σε νέες οδούς για τον έλεγχο της CRSwNP. Τα θεραπευτικά σχήματα για την CRSwNP περιλαμβάνουν πλέον τα βιολογικά φαρμακα. Τον Ιούλιο του 2019, το dupilumab [Dupixent®; Sanofi και Regeneron], ήταν το πρώτο μονοκλωνικό αντίσωμα, το οποίο εγκρίθηκε από το FDA για τη θεραπεία της CRSwNP. Και στη συνέχεια εγκρίθηκε η κυκλοφορία του και στην Ευρωπαϊκή Ένωση. Οι κλινικές μελέτες Φάσης 3 απέδειξαν την αποτελεσματικότητα του dupilumab ως ανταγωνιστή αντι-IL4Ra που αποτρέπει τη δέσμευση της IL-4 και της IL-13 στους υποδοχείς της και αποκλείει τη μεταγενέστερη σηματοδότηση της φλεγμονώδους οδού Τ2.
Αυτές οι μελέτες δείχνουν ότι το dupilumab είναι μια αποδεδειγμένη θεραπευτική επιλογή για τον έλεγχο της νόσου. Συλλογικές μελέτες  καταδεικνύουν υψηλό προφίλ ασφάλειας και μια σημαντική και κλινικής σημασίας μείωση του φορτίου της νόσου, που εκτείνεται από τη μείωση του μεγέθους των πολυπόδων μέχρι τη μείωση των συμπτωμάτων από τους παραρρίνιους κόλπους και τη βελτίωση της όσφρησης. Αυτές οι αλλαγές οδήγησαν διαδοχικά σε σημαντική αύξηση της ποιότητας της ζωής των ασθενών. Τέλος, η βιολογική θεραπεία έναντι της θεραπείας με εικονικό φάρμακο μείωσε την ανάγκη για συστηματική χρήση κορτικοστεροειδών και χειρουργικών επεμβάσεων των παραρρίνιων κόλπων[19].
καταδεικνύουν υψηλό προφίλ ασφάλειας και μια σημαντική και κλινικής σημασίας μείωση του φορτίου της νόσου, που εκτείνεται από τη μείωση του μεγέθους των πολυπόδων μέχρι τη μείωση των συμπτωμάτων από τους παραρρίνιους κόλπους και τη βελτίωση της όσφρησης. Αυτές οι αλλαγές οδήγησαν διαδοχικά σε σημαντική αύξηση της ποιότητας της ζωής των ασθενών. Τέλος, η βιολογική θεραπεία έναντι της θεραπείας με εικονικό φάρμακο μείωσε την ανάγκη για συστηματική χρήση κορτικοστεροειδών και χειρουργικών επεμβάσεων των παραρρίνιων κόλπων[19].
To 2023 o Kei Hosoya, και οι συνεργάτες δημοσίευσαν τα αποτελέσματα της μη παρεμβατικής ανοιχτής μελέτης τους, η οποία διεξήχθη μεταξύ Μαρτίου 2021 και Ιουλίου 2021. Χορήγησαν dupilumab σε ασθενείς με ατοπική δερματίτιδα, βρογχικό άσθμα και χρόνια ρινοκολπίτιδα με ρινικούς πολύποδες, σε 15 θέσεις του σώματος.
Ζητήθηκε από τους ασθενείς να συμπληρώσουν ένα ερωτηματολόγιο , που αφορούσε την αυτοχορήγηση του φαρμάκου, που είχε σχέση με τη συχνότητα και την αποτελεσματικότητα της δοσολογίας, καθώς και τη χρήση και την ικανοποίησή τους με το dupilumab. Τα εμπόδια στη συμμόρφωση αξιολογήθηκαν χρησιμοποιώντας το Adherence Starts with Knowledge-12.
Αυτή η μελέτη συμπεριέλαβε 331 ασθενείς που χρησιμοποίησαν dupilumab για ατοπική δερματίτιδα (n = 164), χρόνια ρινοκολπίτιδα με ρινικούς πολύποδες (n = 102) και βρογχικό άσθμα (n = 65). Η διάμεση αποτελεσματικότητα του dupilumab βαθμολογήθηκε με 9,3 στην οπτική αναλογική κλίμακα.
Συνολικά, το 85,5% των ασθενών έκαναν μόνοι τους την ένεση dupilumab και το 70,7% συμμορφώθηκε απόλυτα με τις καθορισμένες ημερομηνίες ένεσης. Η προγεμισμένη συσκευή τύπου πένας ήταν σημαντικά ανώτερη από τη συμβατική σύριγγα, όσον αφορά τη χρηστικότητα, τη λειτουργικότητα, την ευκολία ώθησης του εμβόλου και την ικανοποίηση του ασθενούς.
Ωστόσο, η προγεμισμένη συσκευή τύπου πένας προκάλεσε περισσότερο πόνο κατά την αυτοένεση από ό,τι η σύριγγα. Η πολυπαραγοντική ανάλυση λογιστικής παλινδρόμησης έδειξε ότι η συμμόρφωση μειώθηκε με μεγαλύτερη διάρκεια θεραπείας με dupilumab (p = 0,017) και δεν συσχετίστηκε με την ηλικία, το φύλο, την υποκείμενη νόσο ή τον τύπο της συσκευής.
Συμπέρασμα: Η προγεμισμένη πένα dupilumab ήταν ανώτερη από τη σύριγγα, όσον αφορά τη χρηστικότητα, τη λειτουργικότητα, την ευκολία ώθησης του εμβόλου και την ικανοποίηση του ασθενούς. Συνιστώνται επαναλαμβανόμενες οδηγίες για την πρόληψη της κακής τήρησης της αυτοένεσης dupilumab[20].
Τα αποτελέσματα της κλινικής έρευνας στη θεραπεία της CRSwNP με μεπολιζουμάμπη [mepolizumab, (Nucala®)]
Το 2021 ο Joseph K Han και οι συνεργάτες δημοσίευσαν τα αποτελέσματα της κλινικής μελέτης SYNAPSE, η οποία ήταν μια τυχαιοποιημένη, διπλά τυφλή μελέτη, ελεγχόμενη με εικονικό φάρμακο και, παράλληλη ομάδα δοκιμής φάσης 3 που έγινε σε 93 κέντρα, κυρίως νοσοκομείων, σε 11 χώρες.
 Οι επιλέξιμοι ασθενείς ήταν ηλικίας 18 ετών και άνω με υποτροπιάζοντα, ανθεκτικά, σοβαρά, αμφοτερόπλευρα συμπτώματα ρινικών πολυπόδων. (βαθμολογία συμπτώματος ρινικής απόφραξης οπτικής αναλογικής κλίμακας [VAS] >5). Οι ασθενείς αυτοί επιλέχτηκαν, διότι χειρουργήθηκαν επανειλημμένως (βαθμολογία VAS συνολικών συμπτωμάτων >7 και ενδοσκοπική βαθμολογία ρινικών πολύποδων ≥5, με ελάχιστο σκορ 2 σε κάθε ρινική κοιλότητα) παρά την τυπική θεραπεία φροντίδας και χρειάστηκε να έχουν υποβληθεί τουλάχιστον σε μία ρινική χειρουργική επέμβαση τα τελευταία 10 χρόνια.
Οι επιλέξιμοι ασθενείς ήταν ηλικίας 18 ετών και άνω με υποτροπιάζοντα, ανθεκτικά, σοβαρά, αμφοτερόπλευρα συμπτώματα ρινικών πολυπόδων. (βαθμολογία συμπτώματος ρινικής απόφραξης οπτικής αναλογικής κλίμακας [VAS] >5). Οι ασθενείς αυτοί επιλέχτηκαν, διότι χειρουργήθηκαν επανειλημμένως (βαθμολογία VAS συνολικών συμπτωμάτων >7 και ενδοσκοπική βαθμολογία ρινικών πολύποδων ≥5, με ελάχιστο σκορ 2 σε κάθε ρινική κοιλότητα) παρά την τυπική θεραπεία φροντίδας και χρειάστηκε να έχουν υποβληθεί τουλάχιστον σε μία ρινική χειρουργική επέμβαση τα τελευταία 10 χρόνια.
Ευρήματα: Από τις 25 Μαΐου 2017 έως τις 12 Δεκεμβρίου 2018, 854 ασθενείς υποβλήθηκαν σε έλεγχο καταλληλότητας. 414 ασθενείς κατανεμήθηκαν τυχαία με 407 να περιλαμβάνονται στον πληθυσμό ITT. 206 έλαβαν mepolizumab και 201 έλαβαν εικονικό φάρμακο. Η συνολική βαθμολογία ενδοσκοπικού ρινικού πολύποδα βελτιώθηκε σημαντικά την εβδομάδα 52 από την αρχική τιμή με το mepolizumab έναντι του εικονικού φαρμάκου (προσαρμοσμένη διαφορά στη διάμεσο -0·73, 95% CI -1·11 έως -0,34· p<0·0001) και βαθμολογία VAS ρινικής απόφραξης κατά τη διάρκεια των εβδομάδων 49-52 επίσης βελτιώθηκε σημαντικά (-3,14, -4,09 έως -2,18, p<0,0001).
Ανεπιθύμητες ενέργειες που θεωρήθηκαν ότι σχετίζονται με τη θεραπεία της μελέτης αναφέρθηκαν σε 30 (15%) από τους 206 ασθενείς που έλαβαν mepolizumab και σε 19 (9%) από τους 201 που έλαβαν εικονικό φάρμακο. Σοβαρές ανεπιθύμητες ενέργειες κατά τη θεραπεία εμφανίστηκαν σε 12 (6%) ασθενείς που έλαβαν mepolizumab και 13 (6%) που έλαβαν εικονικό φάρμακο. Kαμία δεν θεωρήθηκε σχετιζόμενη με τη θεραπεία σε όσους έλαβαν μεπολιζουμάμπη. Ένας θάνατος αναφέρθηκε στην ομάδα του εικονικού φαρμάκου (έμφραγμα του μυοκαρδίου, ο θάνατος σημειώθηκε 99 ημέρες μετά την τελευταία δόση) και θεωρήθηκε ότι δεν σχετίζεται με τη θεραπεία.
Η θεραπεία με mepolizumab βελτίωσε το μέγεθος των ρινικών πολυπόδων και τη ρινική απόφραξη σε σύγκριση με το εικονικό φάρμακο, χωρίς νέες ενδείξεις ασφάλειας, σε ασθενείς με υποτροπιάζουσα, ανθεκτική σοβαρή χρόνια ρινοκολπίτιδα με ρινικούς πολύποδες. [21].
Όπως αναφέρουν, ο Claus Bachert και οι συνεργάτες (2021), αξιολογώντας την αποτελεσματικότητα του mepolizumab σε ασθενείς της κλινική μελέτης SYNAPSE φάσης ΙΙΙ που ομαδοποιούνται με συννοσηρότητα άσθματος, αναπνευστική νόσο επιδεινούμενη από τη λήψη ασπιρίνης (AERD) και αρχικό αριθμό ηωσινοφίλων στο αίμα (BEC), το mepolizumab μείωσε το μέγεθος των πολυπόδων και τη ρινική απόφραξη σε χρόνια ρινοκολπίτιδα με ρινικούς πολύποδες ανεξάρτητα από την παρουσία συννοσηρότητας άσθματος ή AERD [22].
Το mepolizumab (Nucala, GlaxoSmith–Kline) εγκρίθηκε το 2015 για τη θεραπεία του σοβαρού άσθματος με ηωσινόφιλο φαινότυπο. Σε αντίθεση με τη ρεσλιζουμάμπη που δεν χορηγείται σε άτομα κάτω των 18 ετών, η μεπολιζουμάμπη μπορεί να χρησιμοποιηθεί σε εφήβους ηλικίας έως 12 ετών. Η θεραπεία χορηγείται υποδορίως σε δόση 100 mg κάθε τέσσερις εβδομάδες[23]. Το κόστος ενός φιαλιδίου των 100 mg μίας δόσης, στις ΗΠΑ, είναι 3.342 $ [24].
Έχουν αναφερθεί λοιμώξεις από τον έρπητα ζωστήρα με τη χρήση μεπολιζουμάμπης, που προκαλεί ιδιαίτερη ανησυχία για ανοσοκατεσταλμένους ασθενείς που διατρέχουν αυξημένο κίνδυνο λοιμώξεων και δεν πληρούν τις προϋποθέσεις για τον εμβολιασμό κατά του έρπητα ζωστήρα[25].
Τα αποτελέσματα της κλινικής έρευνας στη θεραπεία της CRSwNP με benralizumab (Fasenra®)
Το Benralizumab ( Fasenra®)[26], είναι ένα μονοκλωνικό αντίσωμα που στρέφεται κατά της αλυσίδας άλφα του υποδοχέα  ιντερλευκίνης-5 ( CD125 ). Αναπτύχθηκε από τη MedImmune για τη θεραπεία του άσθματος .
ιντερλευκίνης-5 ( CD125 ). Αναπτύχθηκε από τη MedImmune για τη θεραπεία του άσθματος .
Δύο κλινικές δοκιμές φάσης ΙΙΙ του benralizumab ανέφεραν ότι πληρούσαν τα κύρια καταληκτικά τους σημεία το 2016. Εγκρίθηκε από τον Οργανισμό Τροφίμων και Φαρμάκων των ΗΠΑ τον Νοέμβριο του 2017 για τη θεραπεία του σοβαρού ηωσινοφιλικού άσθματος [27].
Χορηγήθηκε ως ορφανό φάρμακο από τον Οργανισμό Τροφίμων και Φαρμάκων για τη θεραπεία της ηωσινοφιλικής οισοφαγίτιδας τον Αύγουστο του 2019[28].
Το βιολογικό φάρμακο benralizumab που στοχεύει την IL-5 σε ασθενείς με CRSwNP έχει δείξει βελτίωση διαφόρων μετρήσεων, όπως οι βαθμολογία της ρινοκολπικής έκβασης (SNOT-22), βαθμολογία ρινικών πολυπόδων (NPS), βαθμολογία ρινικής συμφόρησης (NCS) και βαθμολογία θολερότητας των παραρρίνιων κόλπων κατά Lund-Mackay. Η αποτελεσματικότητα που αποδείχθηκε μέσω των δοκιμών φάσης 3 και οι post hoc αναλύσεις των μελετών άσθματος φάσης 3 για το benralizumab έχουν επίσης δείξει θετικά αποτελέσματα για τη χρήση βιολογικών φαρμάκων για ασθενείς με CRSwNP[29].
Επειδή η ηωσινοφιλική φλεγμονή έχει εμπλακεί στην παθογένεση, τη σοβαρότητα και την ανταπόκριση στη θεραπεία της χρόνιας ρινοκολπίτιδας με ρινικούς πολύποδες (CRSwNP), ο Claus Bachert και οι συνεργάτες (2022) επεδίωξαν να αξιολογήσουν την αποτελεσματικότητα και την ασφάλεια της μείωσης των ηωσινοφίλων με τη μεσολάβηση του benralizumab για τη θεραπεία της CRSwNP. Στη μελέτη αυτή, την OSTRO, φάσης 3 συμμετείχαν ασθενείς με σοβαρή CRSwNP που ήταν συμπτωματικοί παρά τη θεραπεία με ενδορρινικά κορτικοστεροειδή και που είχαν ιστορικό συστηματικής χρήσης κορτικοστεροειδών ή/και χειρουργικής επέμβασης για ρινικούς πολύποδες. Ο πληθυσμός της μελέτης περιελάμβανε 413 τυχαιοποιημένους ασθενείς (207 στην ομάδα της benralizumab και 206 στην ομάδα του εικονικού φαρμάκου).
Οι ασθενείς τυχαιοποιήθηκαν 1:1 σε θεραπεία με benralizumab 30 mg ή εικονικό φάρμακο κάθε 4 εβδομάδες για τις πρώτες 3 δόσεις και κάθε 8 εβδομάδες στη συνέχεια. Συμπερασματικά, βρέθηκε ότι η μπενραλιζουμάμπη προστέθηκε στη θεραπεία τυπικής φροντίδας, της ρινοκολπίτιδας με πολύποδες μειώθηκαν οι πολύποδες, η ρινική απόφραξη και η δυσκολία στην όσφρηση σε σύγκριση με τα αποτελέσματα των ασθενών με CRSwNP, στους οποίους χορηγήθηκε εικονικό φάρμακο[30].
Τα αποτελέσματα της κλινικής έρευνας στη θεραπεία με Tezepelumab σε ασθενείς με σοβαρό, μη ελεγχόμενο άσθμα με και χωρίς ρινική πολυποδίαση
Το Tezepelumab (tezepelumab-ekko; TEZSPIRE™) είναι ένα μονοκλωνικό αντίσωμα IgG2λ που που συνδέεται με την ανθρώπινη  λεμφοποιητίνη του θυμικού στρώματος (TSLP) και αναστέλλει την αλληλεπίδρασή του με τον υποδοχέα TSLP, όταν χορηγείται υποδορίως. το Tezspire (tezepelumab-ekko) είναι ένα μονοκλωνικό αντίσωμα IgG2λ. Η ανθρώπινη λεμφοποιητίνη του θυμικού στρώματος (TSLP) είναι μια κυτοκίνη που προέρχεται κυρίως από επιθηλιακά κύτταρα και καταλαμβάνει μια ανάντη θέση στον καταρράκτη της φλεγμονής του άσθματος. Αναπτύσσεται από τις φαρμακοβιομηχανίες Amgen και την AstraZeneca για τη θεραπεία του άσθματος, της χρόνιας αποφρακτικής πνευμονοπάθειας (ΧΑΠ), της χρόνιας ρινοκολπίτιδας με ρινικούς πολύποδες (CRSwNP), της χρόνιας αυτόματης κνίδωσης και της ηωσινοφιλικής οισοφαγίτιδας.
λεμφοποιητίνη του θυμικού στρώματος (TSLP) και αναστέλλει την αλληλεπίδρασή του με τον υποδοχέα TSLP, όταν χορηγείται υποδορίως. το Tezspire (tezepelumab-ekko) είναι ένα μονοκλωνικό αντίσωμα IgG2λ. Η ανθρώπινη λεμφοποιητίνη του θυμικού στρώματος (TSLP) είναι μια κυτοκίνη που προέρχεται κυρίως από επιθηλιακά κύτταρα και καταλαμβάνει μια ανάντη θέση στον καταρράκτη της φλεγμονής του άσθματος. Αναπτύσσεται από τις φαρμακοβιομηχανίες Amgen και την AstraZeneca για τη θεραπεία του άσθματος, της χρόνιας αποφρακτικής πνευμονοπάθειας (ΧΑΠ), της χρόνιας ρινοκολπίτιδας με ρινικούς πολύποδες (CRSwNP), της χρόνιας αυτόματης κνίδωσης και της ηωσινοφιλικής οισοφαγίτιδας.
Το Tezepelumab έλαβε την πρώτη του έγκριση στις 17 Δεκεμβρίου 2021 ως συμπληρωματική θεραπεία συντήρησης για ασθενείς ηλικίας ≥ 12 ετών με σοβαρό άσθμα στις ΗΠΑ. Είναι το μόνο βιολογικό εγκεκριμένο για σοβαρό άσθμα χωρίς περιορισμούς φαινοτύπου (π.χ. ηωσινόφιλο ή αλλεργικό) ή βιοδείκτες.
Επί του παρόντος βρίσκεται σε εξέλιξη μια κανονιστική αξιολόγηση του Tezepelumab για τη θεραπεία του άσθματος στην ΕΕ και την Ιαπωνία. Το Tezepelumab έλαβε τον χαρακτηρισμό ορφανού φαρμάκου για τη θεραπεία της ηωσινοφιλικής οισοφαγίτιδας τον Οκτώβριο του 2021 στις ΗΠΑ και βρίσκεται υπό κλινική ανάπτυξη για τη θεραπεία της ΧΑΠ, του CRSwNP και της χρόνιας αυτόματης κνίδωσης[31].
To 2021 η Claire Emson και οι συνεργάτες μελέτησαν εκ των υστέρων ανάλυση της μελέτης PATHWAY Φάσης 2β που αφορούσε την αποτελεσματικότητα του Tezepelumab σε ασθενείς με σοβαρό, μη ελεγχόμενο άσθμα με και χωρίς ρινική πολύποδίαση.
Τα αποτελέσματα αυτής της μελέτης έδειξαν ότι κατά την έναρξη της θεραπείας, οι ασθενείς με ρινικούς πολύποδες (NP+) είχαν υψηλότερο αριθμό ηωσινοφίλων στο αίμα, υψηλότερα επίπεδα κλάσματος εκπνεομένου οξειδίου του αζώτου [fraction of exhaled nitric oxide (FeNO) και υψηλότερα επίπεδα IL-5 και IL-13 στον ορό από τους ασθενείς, που δεν είχαν πολύποδες. Το Tezepelumab, που χορηγήθηκε με υποδόρια ένεση των 210 mg μείωσε τα ετήσια ποσοστά παρόξυνσης του άσθματος (AAER), έναντι του εικονικού φαρμάκου σε παρόμοιο βαθμό σε ασθενείς με NP+ και NP- (NP+, 75% [95% διάστημα εμπιστοσύνης (CI): 15, 93], n=23, NP-, 73% [95% CI: 47, 86], n=112). Οι ασθενείς που έλαβαν Tezepelumab 210 mg εμφάνισαν μεγαλύτερες μειώσεις στον αριθμό των ηωσινοφίλων στο αίμα και στα επίπεδα των FeNO, IL-5 και IL-13 σε σχέση με ασθενείς που έλαβαν εικονικό φάρμακο, ανεξάρτητα από την κατάσταση της ρινικής πολυποδίασης (ΝΡ).
Το Tezepelumab μείωσε τις παροξύνσεις και μείωσε τους φλεγμονώδεις βιοδείκτες τύπου 2 σε ασθενείς με και χωρίς ρινικούς πολύποδες, υποστηρίζοντας την αποτελεσματικότητά του σε έναν ευρύ πληθυσμό ασθενών με σοβαρό άσθμα[32].
H Tanya M Laidlaw και οι συνεργάτες (2023) δημοσίευσαν τα αποτελέσματα της δράσης της Tezepelumab σε ασθενείς με σοβαρό, ανεξέλεγκτο άσθμα με συννοσηρότητα ρινικών πολυπόδων στη μελέτη NAVIGATOR.
1059 ασθενείς με σοβαρό άσθμα τυχαιοποιήθηκαν (1:1) και έλαβαν Tezepelumab 210 mg με υποδόρια ένεση ή εικονικό φάρμακο κάθε 4 εβδομάδες για 52 εβδομάδες. Οι προκαθορισμένες διερευνητικές αναλύσεις περιελάμβαναν: Τα ετήσια ποσοστά παρόξυνσης του άσθματος (AAER) σε υποομάδες ασθενών με ρινικούς πολύποδες, σε διάστημα 52 εβδομάδων και αλλαγές από την έναρξη έως την εβδομάδα 52 στον προ-βρογχοδιασταλτικό εξαναγκασμένο εκπνευστικό όγκο σε 1 δευτερόλεπτο, βαθμολογίες Sino-Nasal Outcome Test (SNOT)-22, και έλεγχο άσθματος και ποιότητας ζωής που σχετίζεται με την υγεία (HRQoL ).
Αξιολογήθηκαν (post hoc) μεταβολές από την αρχική τιμή του κλασματικού εκπνεόμενου μονοξειδίου του αζώτου (FeNO), του αριθμού των ηωσινοφίλων στο αίμα, της ολικής ανοσοσφαιρίνης Ε (IgE), της νευροτοξίνης που προέρχεται από ηωσινόφιλα (EDN), της μεταλλοπρωτεϊνάσης-10 (MMP-10) και της ιντερλευκίνης ορού (IL)-5, IL-6, IL-8 και IL-13.
Τα αποτελέσματα της μελέτης έδειξαν ότι το Tezepelumab μείωσε τις παροξύνσεις του άσθματος (AAER) για 52 εβδομάδες έναντι του εικονικού φαρμάκου κατά 85% (95% διάστημα εμπιστοσύνης [CI]: 72, 92; n=118) και 51% (95% CI: 40, 60, n=941) σε ασθενείς με και χωρίς ρινικούς πολύποδες, αντίστοιχα. Την εβδομάδα 52, το tezepelumab βελτίωσε τη λειτουργία των πνευμόνων, τον έλεγχο του άσθματος και την ποιότητα ζωής που σχετίζεται με την υγεία (HRQoL) έναντι του εικονικού φαρμάκου σε ασθενείς με και χωρίς ρινικούς πολύποδες. Το tezepelumab μείωσε τις συνολικές βαθμολογίες SNOT-22 [Sino-Nasal Outcome Test (SNOT) είναι ένα ευρέως χρησιμοποιούμενο ερωτηματολόγιο για την αξιολόγηση της επίδρασης της χρόνιας ρινοκολπίτιδας (CRS) στην ποιότητα ζωής ενός ασθενούς]. (ελάχιστα τετράγωνα μέση διαφορά έναντι εικονικού φαρμάκου [95% CI]) σε ασθενείς με ρινικούς πολύποδες στις 28 εβδομάδες (-12,57 μονάδες [-19,40, -5,73]) και στις 52 εβδομάδες (-10,58 μονάδες [-17,75 , -3,41]). Την εβδομάδα 52, το tezepelumab μείωσε τον αριθμό των ηωσινοφίλων στο αίμα και τα επίπεδα FeNO, IgE, IL-5, IL-13, EDN και MMP-10 έναντι του εικονικού φαρμάκου, ανεξάρτητα από την κατάσταση των ρινικών πολυπόδων. Το tezepelumab οδήγησε σε κλινικά σημαντικές βελτιώσεις στα ρινικά συμπτώματα και στην έκβαση του άσθματος σε ασθενείς με σοβαρό άσθμα με συνυπάρχοντες ρινικούς πολύποδες[33]. Με αυτήν την εξέλιξη, χωρίς αμφιβολία, ξεκίνησε μια νέα εποχή για τη θεραπεία της σοβαρής ανεξέλεγκτης χρόνιας ρινοκολπίτιδας με ρινικούς πολύποδες.
Τα αποτελέσματα της κλινικής έρευνας στη θεραπεία με reslizumab, [Cinqair®] σε ασθενείς με σοβαρό, μη ελεγχόμενο άσθμα με και χωρίς ρινική πολυποδίαση
Η reslizumab (Cinqair, Teva Pharmaceuticals) είναι ένα μονοκλωνικό αντίσωμα ανταγωνιστής της ιντερλευκίνης (IL)-5, που συνδέεται με την  άλφα αλυσίδα του IL-5 υποδοχέα στην επιφάνεια των ηωσινοφίλων για την αναστολή του πολλαπλασιασμού των ηωσινοφίλων. Η χορήγησή του ενδείκνυται για τη θεραπεία του σοβαρού ηωσινοφιλικού άσθματος. Η IL-5 είναι μια κύρια κυτοκίνη που εμπλέκεται στην ανάπτυξη, διαφοροποίηση, στρατολόγηση, ενεργοποίηση και επιβίωση των ηωσινόφιλων. Οι υποδοχείς IL-5 εκφράζονται στην επιφάνεια των ηωσινοφίλων. Η ρεσλιζουμάμπη συνδέεται με την άλφα αλυσίδα του υποδοχέα IL-5 στην επιφάνεια των ηωσινοφίλων για να αναστείλει τον πολλαπλασιασμό των ηωσινοφίλων. Η εξέλιξη της φλεγμονής πιστεύεται ότι συμβάλλει στην παθογένεση του άσθματος. Μέσω της αναστολής της παραγωγής ηωσινοφίλων και της επιβίωσης, η φλεγμονώδης διαδικασία του άσθματος θεωρητικά μειώνεται.
άλφα αλυσίδα του IL-5 υποδοχέα στην επιφάνεια των ηωσινοφίλων για την αναστολή του πολλαπλασιασμού των ηωσινοφίλων. Η χορήγησή του ενδείκνυται για τη θεραπεία του σοβαρού ηωσινοφιλικού άσθματος. Η IL-5 είναι μια κύρια κυτοκίνη που εμπλέκεται στην ανάπτυξη, διαφοροποίηση, στρατολόγηση, ενεργοποίηση και επιβίωση των ηωσινόφιλων. Οι υποδοχείς IL-5 εκφράζονται στην επιφάνεια των ηωσινοφίλων. Η ρεσλιζουμάμπη συνδέεται με την άλφα αλυσίδα του υποδοχέα IL-5 στην επιφάνεια των ηωσινοφίλων για να αναστείλει τον πολλαπλασιασμό των ηωσινοφίλων. Η εξέλιξη της φλεγμονής πιστεύεται ότι συμβάλλει στην παθογένεση του άσθματος. Μέσω της αναστολής της παραγωγής ηωσινοφίλων και της επιβίωσης, η φλεγμονώδης διαδικασία του άσθματος θεωρητικά μειώνεται.
Το Reslizumab δεν ενδείκνυται για χρήση σε ασθενείς ηλικίας κάτω των 18 ετών. Η ασφάλεια και η αποτελεσματικότητα δεν έχουν τεκμηριωθεί σε αυτόν τον πληθυσμό. Κλινικές μελέτες που αξιολόγησαν 39 ασθενείς ηλικίας 12 ετών έως κάτω των 18 ετών κατέδειξαν υψηλότερο ποσοστό παροξύνσεων για τους εφήβους που έλαβαν θεραπεία με ρεσλιζουμάμπη σε σύγκριση με το εικονικό φάρμακο.
Η ένεση ρεσλιζουμάμπης για ενδοφλέβια (IV) χρήση, είναι ο νεότερος ανοσοτροποποιητής συντήρησης που εγκρίθηκε από τον Οργανισμό Τροφίμων και Φαρμάκων (FDA) το 2016[34]. Το Reslizumab διατίθεται σε φιαλίδια μιας χρήσης των 100 mg/10-mL (10 mg/mL) και χορηγείται ενδοφλέβια με βάση το βάρος του ασθενούς (3 mg/kg). Είναι εγκεκριμένο για ασθενείς ηλικίας 18 ετών και άνω[35].
Η μέση τιμή χονδρικής (AWP) για ένα φιαλίδιο είναι 1.032 $. Ένας υποθετικός ασθενής βάρους 90 κιλών θα χρειαζόταν μηνιαία δόση 270 mg, η οποία θα απαιτούσε το περιεχόμενο τριών φιαλιδίων με συνολικό κόστος 3.096 $ (με την περίσσεια του φαρμάκου να απορρίπτεται)[36].
Το Reslizumab φέρει μια προειδοποίηση σε κουτί για αναφυλαξία. Ως εκ τούτου, οι ασθενείς θα χρειαστούν χορήγηση φαρμάκου και επακόλουθη παρακολούθηση από έναν επαγγελματία υγείας που είναι σε θέση να αντιμετωπίσει μια αναφυλακτική αντίδραση. Κακοήθειες και αύξηση της CPK έχουν επίσης αναφερθεί με τη χρήση ρεσλιζουμάμπης[37].
Παρενέργειες της βιολογικής θεραπείας της χρόνιας ρινοκολπίτιδας με ρινικούς πολύποδες
Το 2022 ο Ahmad Aldajani και οι συνεργάτες διεξήγαγαν μια ολοκληρωμένη συστηματική ανασκόπηση σχετικά με την ασφάλεια των διαφορετικών βιολογικών θεραπειών, όταν χρησιμοποιούνται για τη διαχείριση της CRSwNP. Συμπεριέλαβαν στην ανασκόπησή τους 12 τυχαιοποιημένες ελεγχόμενες δοκιμές (RCT) και μίας συγχρονική μελέτη. Το συνολικό μέγεθος του δείγματος για τις συμπεριλαμβανόμενες μελέτες ήταν 2282 ασθενείς. Έξι μελέτες διερεύνησαν την ασφάλεια και τις ανεπιθύμητες ενέργειες του dupilumab. Τρεις διερεύνησαν το omalizumab, τρεις διερεύνησαν το mepolizumab και μόνο μία διερεύνησε το reslizumab. Ορισμένες μελέτες είχαν αναφέρει ότι οι ανεπιθύμητες ενέργειες ήταν κοινές με αυτούς τους τύπους φαρμάκων. Ωστόσο, δεν ήταν συγκεκριμένες και αυτοπεριοριζόμενες. Οι πονοκέφαλοι, οι αντιδράσεις στο σημείο της ένεσης και η φαρυγγίτιδα ήταν οι πιο συχνές ανεπιθύμητες ενέργειες που βρέθηκαν μεταξύ των αναφερόμενων ανεπιθύμητων ενεργειών.
Η κλινική μελέτη του Dupilumab ανέφερε φαρυγγίτιδα σε 225 ασθενείς (22,4 %) ακολουθούμενη από ερύθημα στο 9,4 %, πονοκέφαλο στο 8,1 %, επίσταξη στο 5,1 %, και άσθμα στο 1,7 % των ασθενών. Οι κλινικές μελέτες που χρησιμοποίησαν το omalizumab ανέφεραν πονοκεφάλους, ρινική φαρυγγίτιδα, αντιδράσεις στο σημείο της ένεσης ως τις πιο συχνές ανεπιθύμητες ενέργειες με εκτιμώμενα ποσοστά επιπολασμού 8,1 %, 5,9 % και 5,2 % αντίστοιχα. Οι κλινικές μελέτες mepolizumab και reslizumab ανέφεραν ότι το 40% των ασθενών είχαν επιπλοκές από ρινικούς πολύποδες/συμφόρηση/φαρυγγίτιδα/λοιμώξεις, 14 είχαν πονοκέφαλο (15,5 %), δύο εμφάνισαν άσθμα (2,2 %) και μόνο ένας ασθενής (1,1 %) είχε επίσταξη ως ένα ανεπιθύμητο συμβάν. Αν και οι τρέχουσες έρευνες της βιβλιογραφίας υποδεικνύουν την ασφάλεια της θεραπείας με τους βιολογικούς παράγοντες, εν τούτοις απαιτούνται περαιτέρω μελέτες καθώς έχει αναφερθεί κάποια αβεβαιότητα μεταξύ των κλινικών μελετών[38].
Το Benralizumab (Fasenra), το dupilumab (Dupixent), το Mepolizumab (Nucala), το omalizumab (Xolair) και το Reslizumab (Cinqair) είναι βιολογικές θεραπείες που έχουν εγκριθεί από τον Οργανισμό Τροφίμων και Φαρμάκων (FDA) για τη θεραπεία του άσθματος. Το dupilumab, το mepolizumab και το omalizumab είναι επίσης εγκεκριμένα για τη θεραπεία των ρινικών πολυπόδων. Τα βιολογικά φάρμακα αποτρέπουν τη φλεγμονή στοχεύοντας τις οδούς ανοσοσφαιρίνης Ε (IgE), ιντερλευκίνης-4 (IL-4), ιντερλευκίνης-5 (IL-5) ή ιντερλευκίνης-13 (IL-13) που σχετίζονται με τις οδούς Th2 και τις ηωσινοφιλικές διαταραχές. Θεωρείται ότι τα βιολογικά που στοχεύουν τις οδούς φλεγμονής στο άσθμα μπορεί να είναι χρήσιμοι φαρμακολογικοί παράγοντες για τη θεραπεία των ρινικών πολύποδων λόγω των αυξημένων επιπέδων ιντερλευκίνης που επιδεικνύονται σε ασθενείς με ρινικούς πολύποδες. Θα πρέπει να υπάρχει φλεγμονή τύπου 2 για τη χρήση βιολογικών στο CRSwNP[39]. Η ιντερλευκίνη-16 (IL-16), μια άλλη κυτοκίνη ανοσοδιαμορφωτής που υπάρχει στο άσθμα και άλλες αυτοάνοσες ασθένειες, έχει σημαντική αύξηση σε ασθενείς με ρινικούς πολύποδες και μπορεί να είναι υπεύθυνη για τη μετανάστευση των ηωσινοφίλων και την ανάπτυξη ρινικών πολυπόδων. Τα βιολογικά φάρμακα που στοχεύουν την IL-16 μπορεί να αποτρέψουν τη μετανάστευση και την ενεργοποίηση των ηωσινοφίλων και μπορεί να αποτελέσουν μια πιθανή μελλοντική θεραπεία για τη θεραπεία των ρινικών πολυπόδων[40]. Η απόφαση για τη χορήγηση ενός από τους διαθέσιμους βιολογικούς παράγοντες σε ασθενείς με χρόνια ρινοκολπίτιδα με ρινικούς πολύποδες λαμβάνεται, αφού έχει ερευνηθεί ο ασθενής για το ποια κυτοκίνη ευθύνεται για την πρόκληση ή τη συντήρηση της νόσου. Επίσης πρέπει να μετρώνται στον ορό οι ολικές IgE και οι ειδικές ΙgΕ που ευθύνονται για τη δημιουργία της νόσου και να καθορίζονται οι τρόποι φροντίδας των ασθενών για την παρακολούθηση της αποτελεσματικότητας των βιολογικών παραγόντων σε μεμονωμένους ασθενείς, ώστε να ενσωματώνουν το ισχύον πρότυπο θεραπευτικής φροντίδας, συμπεριλαμβανομένης της χειρουργικής [41], αναμένοντας τη μείωση ή την εξαφάνιση των ρινικών πολυπόδων και την υποχώρηση του σοβαρού συνυπάρχοντος άσθματος[42].
H αντιμετώπιση της χρόνιας ρινοκολπίτιδας με ρινικούς πολύποδες με μικκυλιακή κουρκουμίνη (Curcugkel).
Η εισαγωγή των βιολογικών φαρμάκων άνοιξε έναν νέο δρόμο στη θεραπευτική αντιμετώπιση της χρόνιας ρινοκολπίτιδας με ή χωρίς πολύποδες και με ή χωρίς άσθμα. Όμως η αποτελεσματικότητα τους δεν γίνεται εμφανής άμεσα και σύντομα. Επιπλέον, υπάρχουν φαίνεται και άλλες κυτοκίνες, που συμμετέχουν στη δημιουργία της φλεγμονής, όπως π.χ. η IL-16 και η ΙL-17, των οποίων η δράση δεν έχει βρεθεί ακόμη ότι αναστέλλεται από κάποιο από τα κυκλοφορούντα φάρμακα.
Γιαυτό το λόγο, οι ασθενείς ταυτόχρονα με τη λήψη του βιολογικού φαρμάκου συνεχίζουν να παίρνουν από το στόμα κάποιο κορτικοστεροειδές, και να εφαρμόζουν ενδορρινικά κορτικοστεροειδή, αφού καθαρίζουν τις ρινικές εκκρίσεις τους με υπέρτονο διάλυμα φυσιολογικού ορού, μέχρις ότου γίνουν εμφανή τα θεραπευτικά αποτελέσματα του βιολογικού φαρμάκου.
Συμπληρωματικά με την παραπάνω συμβατική, αλλά και τη βιολογική θεραπεία οι ασθενείς που πάσχουν από χρονία ρινοκολπίτιδα με πολύποδες και άσθμα ή χωρίς άσθμα, έχει βρεθεί ότι προκαλεί θεραπευτικά αποτελέσματα, αναχαιτίζοντας τη φλεγμονή και συρρικνώνοντας τους ρινικούς πολύποδες ή καθημερινή λήψη μιας κάψουλας μικκυλιακής κουρκουμίνης (Curcugkel) πρωί και βράδυ με το φαγητό.
H κουρκουμίνη είναι το ενεργό συστατικό της ξηρής σκόνης του ριζώματος του φυτού κουρκουμάς (Curcuma longa), της οποίας η ισχυρή αντιοξειδωτική και αντιφλεγμονώδης δράση έχει αποδειχτεί και επιβεβαιωθεί με εκατοντάδες ερευνητικές εργασίες.
Πολλές προκλινικές και κλινικές μελέτες αποκάλυψαν ότι η κουρκουμίνη διαμορφώνει αρκετά μόρια στην οδό μεταγωγής σήματος κυττάρων συμπεριλαμβανομένων των PI3K, Akt, mTOR, ERK5, AP-1, TGF-β, Wnt, β-catenin, Shh, PAK1, Rac1, STAT3, PPARγ, EBPa, NLRP3 φλεγμονοσωμάτιο (inflammasome), p38MAPK, Nrf2, Notch-1, AMPK, TLR-4 και MyD-88.
Η κουρκουμίνη έχει τη δυνατότητα να προλαμβάνει και / ή να διαχειρίζεται διάφορες ασθένειες λόγω των αντιφλεγμονωδών, αντιοξειδωτικών[44] και αντι-αποπτωτικών ιδιοτήτων της με εξαιρετικό προφίλ ασφάλειας[45]. Η κουρκουμίνη δρα ευεργετικά κατά του άσθματος, αλλά και κατά της ρινοκολπίτιδας με ή χωρίς ρινικούς πολύποδες, καθώς αναστέλλει τα φλεγμονώδη μόρια και τις οδούς που εμπλέκονται στο άσθμα, δυνητικά μειώνοντας τη φλεγμονή και την υπερέκκριση βλέννας των αεραγωγών και βελτιώνοντας την αναπνοή. Η κουρκουμίνη, ηρεμώντας τη φλεγμονώδη απόκριση στους αεραγωγούς μπορεί να βοηθήσει στην ανακούφιση των συμπτωμάτων του άσθματος και στην ενίσχυση της αναπνευστικής λειτουργίας[46].
Η συμπληρωματική χορήγηση κουρκουμίνης βοηθάει στη βελτίωση της απόφραξης των αεραγωγών και αυτό φαίνεται από τη σημαντική βελτίωση στις μέσες τιμές FEV1. Προκαλεί επίσης σημαντική βελτίωση στις αιματολογικές παραμέτρους και η απουσία κλινικά σημαντικών ανεπιθύμητων ενεργειών από τη δράση της υποδηλώνει το αξιόπιστο προφίλ ασφάλειας της[47]. Η κουρκουμίνη συρρικνώνει τους ρινικούς πολύποδες ασκώντας αντιφλεγμονώδη, αντιοξειδωτική και συρρικνωτική δράση.
- Αντιφλεγμονώδης δράση:Η κουρκουμίνη αναστέλλει τη δράση ποικίλων χημικών μεσολαβητών της φλεγμονής και ιδιαίτερα των ιντερλευκινών (π.χ η IL-17) , προλαβαίνοντας έτσι την εξέλιξη της φλεγμονής στους πολύποδες[48]. Η κουρκουμίνη δρα σε μοριακό επίπεδο και αποκλείει τη δημιουργία του παράγοντα NF-KB, το γονίδιο του οποίου ευθύνεται για την ενεργοποίηση του μηχανισμού της φλεγμονής και παρεμποδίζοντας αποτελεσματικά την φλεγμονή των πολυπόδων[49].
Στην παραγωγή της φλεγμονής της CRSwNP συμμετέχει και η IL-17. Τα βοηθητικά Τ- κύτταρα 17 [T-helper 17 (Th17)], είναι ένα μοναδικό υποσύνολο CD4 + Τ-κυττάρων που χαρακτηρίζεται από παραγωγή ιντερλευκίνης-17 (IL-17). Η φλεγμονή που σχετίζεται με τα Th17 είναι αυξημένη στη χρόνια ρινοκολπίτιδα με ρινικό πολύποδα (CRSwNP) και σχετίζεται με τη σοβαρότητα της νόσου και την αντίσταση στα στεροειδή. Η υπερεκφρασμένη ιντερλευκίνη της (IL)-17A επηρεάζει την CRSwNP με αναδιαμόρφωση ιστού, ηωσινόφιλη συσσώρευση και ουδετερόφιλη διήθηση. Η IL-17A πιθανώς παίζει ρόλο στην παθογένεση του CRSwNP, με την κύρια κυτταρική πηγή να είναι τα Μ1 μακροφάγα στους ιστούς των ρινικών πολυπόδων. Τα μακροφάγα είναι μια διαφορετική ομάδα λευκών αιμοσφαιρίων που είναι γνωστά για την εξάλειψη των παθογόνων μέσω της φαγοκυττάρωσης. Τα μακροφάγα Μ1 ενεργοποιούνται κλασικά, τυπικά από IFN-γ ή λιποπολυσακχαρίτη (LPS), και παράγουν προφλεγμονώδεις κυτοκίνες, φαγοκυτταροποιούν τα μικρόβια και ξεκινούν μια ανοσοαπόκριση. Τα μακροφάγα Μ1 παράγουν μονοξείδιο του αζώτου (NO) ή ενδιάμεσα ενεργού οξυγόνου (ROI) για προστασία από βακτήρια και ιούς. Έχει βρεθεί ότι η αυξημένη παραγωγή IL-17A και η ουδετεροφιλία των ιστών σχετίζεται με την αύξησης τη έκφρασης του mRNA και της αύξησης των επιπέδων του HIF-1(Hypoxia-inducible factor 1-alpha) στους ιστούς των πολυπόδων. Ο HIF-1α σχετίζεται με ουδετεροφιλική φλεγμονή και αντίσταση στα γλυκοκορτικοειδή σε ασθενείς με CRSwNP[50].
Η άμεση ή έμμεση στόχευση της IL-17A μπορεί να είναι μια αποτελεσματική θεραπευτική στρατηγική για την CRSwNP[51]. Η κουρκουμίνη αναστέλλει τη διαφοροποίηση και ανάπτυξη των Th17, που συμμετέχουν στη δημιουργία της φλεγμονής των ρινικών πολυπόδων και του άσθματος. Επειδή η φλεγμονή προκαλεί κατακράτηση υγρού στους ιστούς, δημιουργώντας οίδημα και αύξηση του μεγέθους των πολυπόδων, η αντιφλεγμονώδης δράση της κουρκουμίνης ανακόπτει την αύξηση του μεγέθους των πολυπόδων[52].
- Αντιοξειδωτική δράση:Η ισχυρή αντιοξειδωτική ιδιότητα της κουρκουμίνης προλαβαίνει τη δημιουργία ελεύθερων ριζών, οι οποίες είναι μόρια υψηλής αντιδραστικότητας και προκαλούν οξειδωτική βλάβη στους ιστούς. Η οξειδωτική βλάβη έχει προταθεί ως ένας από τους σημαντικότερους μηχανισμούς δημιουργίας των ρινικών πολυπόδων. Καταστέλλοντας τη δημιουργία ελεύθερων ριζών η κουρκουμίνη ανακόπτει την ανάπτυξη των πολυπόδων εν τη γενέσει τους[61].
- Συρρικνωτική δράση:Ίσως, η σημαντικότερη δράση της κουρκουμίνης είναι η ικανότητά της να συρρικνώνει και έτσι να μειώνει το μέγεθος των ρινικών πολυπόδων. Αυτό αποδίδεται στην ικανότητα της κουρκουμίνης να αναστέλλει τη δράση του STAT3. Οι πρωτεΐνες του Μετατροπέα Σήματος και του Ενεργοποιητή Μεταγραφής (STAT)-5 απαιτούνται για τη ρύθμιση του ανοσοποιητικού και την ομοιόσταση και διαδραματίζουν κρίσιμο ρόλο στην ανάπτυξη και λειτουργία πολλών αιμοποιητικών κυττάρων. Η ενεργοποίηση του STAT5b εμπλέκεται στην έκφραση γονιδίων που συμμετέχουν στην ανάπτυξη, τον πολλαπλασιασμό και την επιβίωση των κυττάρων[53]. Είναι πιθανό το STAT5b να συμβάλλει στην ανάπτυξη ρινικών πολυπόδων. Ο STAT3 (Signal transducer and activator of transcription 3) είναι ένας μεταγραφικός παράγοντας, ο οποίος κωδικοποιεί στους ανθρώπους το γονίδιο STAT3 και αποτελεί μέλος της οικογένειας των πρωτεϊνών STAT. Το STAT3 (μετατροπέας σήματος και ενεργοποιητής της μεταγραφής 3) είναι μια φωσφοκινάση και ένα βασικό μόριο σηματοδότησης που εμπλέκεται στη ρύθμιση του κυτταρικού κύκλου[54].

Η ενεργοποιημένη μορφή του pSTAT3 παίζει καθοριστικό ρόλο στην πολλαπλασιαστική ανάπτυξη των ρινικών πολυπόδων[55]. O STAT3 αποκλείει την απόπτωση (προγραμματισμένος κυτταρικός θάνατος) των ρινικών πολυπόδων. Απενεργοποιώντας η κουρκουμίνη τον STAT3 βοηθάει στην προαγωγή της της θανάτωσης των ιστών, από τους οποίους δομούνται οι πολύποδες[56].Η κουρκουμίνη για να δράσει συρρικνωτικά ή και να εξαφανίσει τους ρινικούς πολύποδες πρέπει να χορηγηθεί από το στόμα υπό μορφή καψουλών ή δισκίων, αλλά σε μεγάλες καθημερινές δόσεις των 8-12 γραμμαρίων[57, 58].
Η ανάγκη χορήγησης μεγάλων δόσεων οφείλεται στο γεγονός ότι η φυσική σκόνη κουρκουμίνης διαθέτει πολύ πτωχή απορροφητικότητα από το έντερο και αποβάλλεται ταχύτατα από τον οργανισμό.Αυτή η δοσολογία της κουρκουμίνης είναι πρακτικά ανεφάρμοστη και συνοδεύεται από γαστρεντερικές διαταραχές. Η χορήγηση κουρκουμίνης μαζί με πιπερίνη μπορεί να αυξήσει την απορρόφηση της κουρκουμίνης κατά 2000% [59]. Όμως, η υγρή μικκυλιακή κουρκουμίνη [Curcugkel] είναι 18.500% πιο ευαπορρόφητη και βιοδιαθέσιμη από την απλή σκόνη φυσικής κουρκουμίνης[60]. Μία κάψουλα υγρής μικκυλιακής κουρκουμίνης Curcugkel περιέχει 670 mg Novasol® Curcumin, ήτοι: 36 mg καθαρής ευαπορρόφητης και βιοδιαθέσιμης κουρκουμίνης), η οποία ισοδυναμεί με 7400 mg ή περίπου 16 κάψουλες φυσικής σκόνης κουρκουμίνης ή 185 g σκόνης ρίζας. Για την αντιμετώπιση των ρινικών πολυπόδων χορηγείται μία κάψουλα Curcugkel πρωί, μεσημέρι και βράδυ για τρείς μήνες και στη συνέχεια μια κάψουλα ημερησίως μέχρις ότου εμφανιστούν τα θεραπευτικά αποτελέσματα του βιολογικού φαρμάκου, που χορηγείται και αυτό κατά τακτά χρονικά διαστήματα, που μπορεί να διαρκέσουν από 6-32 μήνες.
Βιβλιογραφική Τεκμηρίωση
1.Fokkens W.J., Lund V.J., Hopkins C., Hellings P.W., Kern R., Reitsma S., et al. European Position Paper on Rhinosinusitis and Nasal Polyps 2020. Rhinology. 2020;58:1–464
2.DeConde A.S., Mace J.C., Levy J.M., Rudmik L., Alt J.A., Sm
ith T.L. Prevalence of polyp recurrence after endoscopic sinus surgery for chronic rhinosinusitis with nasal polyposis. Laryngoscope. 2017;127:550–555.
3.Damask C.C., Ryan M.W., Casale T.B., Castro M., Franzese C.B., Lee S.E., et al. Targeted Molecular Therapies in Allergy and Rhinology. Otolaryngol Head Neck Surg. 2021;164:S1–S21.
4.Jean Kim, Robert Naclerio .Therapeutic Potential of Dupilumab in the Treatment of Chronic Rhinosinusitis with Nasal Polyps: Evidence to Date. Ther Clin Risk Manag. 2020 Jan 23;16:31-37.
5.Matthew R Elliott, Charles E Grogan, Gailen D Marshall. An Update on Monoclonal Antibody Therapy to Treat Moderate-to-Severe Asthma: Benefits, Choices, and Limitations. Am J Med. 2023 Aug;136(8):738-744.
6.Porsbjerg C, Melén E, Lehtimäki L, Shaw D. Asthma. Lancet. 2023 Mar 11;401(10379):858-873.
7.Sergio E Chiarella , Hendrik Sy, Anju T Peters. Monoclonal antibody therapy in sinonasal disease. Am J Rhinol Allergy. 2017 Mar 1;31(2):93-95.
8.William W Busse, Mario Castro, Thomas B Casale. Asthma Management in Adults. J Allergy Clin Immunol Pract. 2023 Jan;11(1):21-33.
9.Naruhito Iwasaki. [Th2 cells and macrophages induce novel type-I-hypersensitivity-like reaction]. Nihon Yakurigaku Zasshi. 2020;155(6):369-374.
10.Melina S Nasta , Vasileios A Chatzinakis , Christos C Georgalas. Updates on current evidence for biologics in chronic rhinosinusitis. Curr Opin Otolaryngol Head Neck Surg. 2020 Feb;28(1):18-24.
11.William W Busse, Mario Castro, Thomas B Casale. Asthma Management in Adults. J Allergy Clin Immunol Pract. 2023 Jan;11(1):21-33.
11.Chen YJ, Chai XB. [Progress of monoclonal antibody treatment for chronic rhinosinusitis with or without nasal polyps]. Lin Chung Er Bi Yan Hou Tou Jing Wai Ke Za Zhi. 2018 May;32(10):789-793.
12.Difficult-to-treat & severe asthma in adolescent and adult patients diagnosis and management. Global Initiative for Asthma website. ginasthma.org/wp-content/uploads/2019/04/GINA-Severe-asthma- Pocket-Guide-v2.0-wms-1.pdf. Published April 2019. Accessed March 13, 2020.
13.Asthma. In: Wells BG, DiPiro JT, Schwinghammer TL, DiPiro CV, eds.Pharmacotherapy Quick Guide. 10th ed. New York, NY: McGraw-Hill; 2017.
14.Galanter JM, Boushey HA. Drugs used in asthma. In: Katzung BG, ed. Basic & Clinical Pharmacology. 14th ed. New York, NY: McGraw-Hill; 2018.
15.Roufosse F. Targeting the interleukin-5 pathway for treatment of eosinophilic conditions other than asthma. Front Med (Lausanne). 2018;5:49. doi: 10.3389/fmed.2018.00049.
16.Diego Bagnasco , Matteo Ferrando , Gilda Varricchi , Francesca Puggioni , Giovanni Passalacqua , Giorgio Walter Canonica Anti-Interleukin 5 (IL-5) and IL-5Ra Biological Drugs: Efficacy, Safety, and Future Perspectives in Severe Eosinophilic Asthma. Front Med (Lausanne) . 2017 Aug 31;4:135.
17.Philippe Gevaert, Theodore A Omachi, Jonathan Corren, Joaquim Mullol, Joseph Han , Stella E Lee, Derrick Kaufman, Monica Ligueros-Saylan, Monet Howard, Rui Zhu , Ryan Owen, Kit Wong, Lutaf Islam, Claus Bachert. Efficacy and safety of omalizumab in nasal polyposis: 2 randomized phase 3 trials. J Allergy Clin Immunol. 2020 Sep;146(3):595-605.
18.Xolair (omalizumab) prescribing information. South San Francisco, California: Genentech USA, Inc; 2003.
19.Jean Kim, Robert Naclerio. Therapeutic Potential of Dupilumab in the Treatment of Chronic Rhinosinusitis with Nasal Polyps: Evidence to Date. Ther Clin Risk Manag. 2020 Jan 23;16:31-37.
20.Kei Hosoya, Taro Komachi, Katsunori Masaki, Isao Suzaki, Hidehisa Saeki, Naoko Kanda, Makoto Nozaki, Yosuke Kamide, Yoshinori Matsuwaki, Yoshiki Kobayashi, Eriko Ogino, Shin-Ichi Osada, Norihiro Usukura, Toshikazu Kurumagawa, Junya Ninomia, Mikiya Asako, Keitaro Nakamoto, Hidenori Yokoi, Manabu Ohyama, Keiji Tanese, Sho Kanzaki, Koichi Fukunaga, Motohiro Ebisawa, Kimihiro Okubo. Barrier Factors of Adherence to Dupilumab Self-Injection for Severe Allergic Disease: A Non-Interventional Open-Label Study. Patient Prefer Adherence. 2023 Mar 27;17:861-872.
21.Joseph K Han, Claus Bachert, Wytske Fokkens, Martin Desrosiers, Martin Wagenmann, Stella E Lee, Steven G Smith, Neil Martin, Bhabita Mayer, Steven W Yancey , Ana R Sousa, Robert Chan, Claire Hopkins; SYNAPSE study investigators. Mepolizumab for chronic rhinosinusitis with nasal polyps (SYNAPSE): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Respir Med. 2021 Oct;9(10):1141-1153.
22.Bachert C, Sousa AR, Han JK, Schlosser RJ, Sowerby LJ, Hopkins C, Maspero JF, Smith SG, Kante O, Karidi-Andrioti DE, Mayer B, Chan RH, Yancey SW, Chaker AM. Mepolizumab for chronic rhinosinusitis with nasal polyps: Treatment efficacy by comorbidity and blood eosinophil count. J Allergy Clin Immunol. 2022 May;149(5):1711-1721.e6.
23.Nucala (mepolizumab) prescribing information. Philadelphia, Pennsylvania: GlaxoSmithKline LLC; 2015.
24.Red Book Online. Ann Arbor, Michigan: Truven Health Analytics; [Accessed July 19, 2017].
25.Pavord ID, Bel EH, Bourdin A, Chan R, Han JK, Keene ON, Liu MC, Martin N, Papi A, Roufosse F, Steinfeld J, Wechsler ME, Yancey SW. From DREAM to REALITI-A and beyond: Mepolizumab for the treatment of eosinophil-driven diseases. Allergy. 2022 Mar;77(3):778-797.
26 “Fasenra EPAR”. European Medicines Agency (EMA). Retrieved 13 October 2020.
27.”Fasenra (benralizumab) receives US FDA approval for severe eosinophilic asthma”. AstraZeneca. 2017-11-14.
28.”Fasenra granted US Orphan Drug Designation for eosinophilic oesophagitis”. www.astrazeneca.com. Retrieved 2019-10-29.
29.Bob Geng, Michelle Dilley, Christine Anterasian. Biologic Therapies for Allergic Rhinitis and Nasal Polyposis. Curr Allergy Asthma Rep. 2021 Jun 10;21(6):36.
30.Claus Bachert, Joseph K Han, Martin Y Desrosiers, Philippe Gevaert, Enrico Heffler, Claire Hopkins, Jody R Tversky, Peter Barker, David Cohen, Claire Emson, Ubaldo J Martin, Vivian H Shih, Sofia Necander, James L Kreindler, Maria Jison, Viktoria Werkström. Efficacy and safety of benralizumab in chronic rhinosinusitis with nasal polyps: A randomized, placebo-controlled trial J Allergy Clin Immunol. 2022 Apr;149(4):1309-1317.e12.
31.Sheridan M Hoy. Tezepelumab: First Approval. Drugs. 2022 Mar;82(4):461-468.
32.Claire Emson, Jonathan Corren, Kinga Sałapa, Åsa Hellqvist, Jane R Parnes, Gene Colice. Efficacy of Tezepelumab in Patients with Severe, Uncontrolled Asthma with and without Nasal Polyposis: A Post Hoc Analysis of the Phase 2b PATHWAY Study. J Asthma Allergy. 2021 Feb 3:14:91-99.
33.Tanya M Laidlaw, Andrew Menzies-Gow, Scott Caveney, Joseph K Han, Nicole Martin, Elliot Israel, Jason K Lee, Jean-Pierre Llanos, Neil Martin, Ayman Megally, Bhavini Parikh, Sylvia Vong, Tobias Welte, Jonathan Corren. Tezepelumab Efficacy in Patients with Severe, Uncontrolled Asthma with Comorbid Nasal Polyps in NAVIGATOR J. Asthma Allergy. 2023 Sep 4:16:915-932.
34. Markham A. Reslizumab: First Global Approval..Drugs. 2016 May;76(8):907-11.
35.Cinqair (reslizumab) prescribing information. Frazer, Pennsylvania: Teva Respiratory LLC; 2016.
36.Red Book Online. Ann Arbor, Michigan: Truven Health Analytics; [Accessed July 19, 2017].
37.Nair P, Bardin P, Humbert M, Murphy KR, Hickey L, Garin M, Vanlandingham R, Chanez P. Efficacy of Intravenous Reslizumab in Oral Corticosteroid-Dependent Asthma.J Allergy Clin Immunol Pract. 2020 Feb;8(2):555-564.
38.Ahmad Aldajani, Ahmad Alroqi, Saud Alromaih, Mohammad O Aloulah, Saad Alsaleh .Adverse events of biological therapy in chronic rhinosinusitis with nasal polyps: A systematic review. Am J Otolaryngol. 2022 Nov-Dec;43(6):103615.
39.Renee R. Koski, PharmD, CACP, FMPA, Luke Hill, PharmD, and Kylee Taavola, PharmD3.Efficacy and Safety of Biologics for Chronic Rhinosinusitis With Nasal Polyps. J Pharm Technol. 2022 Oct; 38(5): 289–296.
40.Lackner A, Raggam RB, Stammberger H, et al. The role of interleukin-16 in eosinophilic chronic rhinosinusitis. Eur Arch Otorhinolaryngol. 2007;264(8):887-993.
41.Bachert C, Zhang N, Cavaliere C, Weiping W, Gevaert E, Krysko O. Biologics for chronic rhinosinusitis with nasal polyps. J Allergy Clin Immunol. 2020 Mar;145(3):725-739.
42.Alexander Rivero1, Jonathan Liang1 Anti-IgE and Anti-IL5 Biologic Therapy in the Treatment of Nasal Polyposis: A Systematic Review and Meta-analysis. Ann Otol Rhinol Laryngol. 2017 Nov;126(11):739-747.
43.Patel SS, Acharya A, Ray RS, Agrawal R, Raghuwanshi R, Jain P. Cellular and molecular mechanisms of curcumin in prevention and treatment of disease. Crit Rev Food Sci Nutr. 2020;60(6):887-939.
44.Menon VP, Sudheer AR. Antioxidant and anti-inflammatory properties of curcumin. .Adv Exp Med Biol. 2007;595:105-25.
45.Haryuna TS, Purba AH, Farhat F, Alviandi W. The Antiapoptotic Effect of Curcumin in the Fibroblast of the Cochlea in an Ototoxic Rat Model. Iran J Otorhinolaryngol. 2018 Sep;30(100):247-253.
46.Zhu T, Chen Z, Chen G, Wang D, Tang S, Deng H, Wang J, Li S, Lan J, Tong J, Li H, Deng X, Zhang W, Sun J, Tu Y, Luo W, Li C. Curcumin Attenuates Asthmatic Airway Inflammation and Mucus Hypersecretion Involving a PPARγ-Dependent NF-κB Signaling Pathway In Vivo and In Vitro. Mediators Inflamm. 2019 Apr 3;2019:4927430.
47.Afroz Abidi, Surabhi Gupta, Manu Agarwal, H L Bhalla, Mahip Saluja . Evaluation of Efficacy of Curcumin as an Add-on therapy in Patients of Bronchial Asthma. J Clin Diagn Res. 2014 Aug;8(8):HC19-24.
48.Ghandadi M, Sahebkar A. Curcumin: An Effective Inhibitor of Interleukin-6. Curr Pharm Des. 2017;23(6):921-931.
49.Singh S, Aggarwal BB. Activation of transcription factor NF-κB is suppressed by curcumin (diferuloylmethane). Journal of Biological Chemistry. 1995 Oct 20;270(42):24995-5000.
50.Yu Z, Wang Y, Hu X, Xu H, Han M, Zhang J, Wen W, Shu H, Li H.Overexpression of hypoxia-inducible factor 1α is associated with neutrophilic inflammation in chronic rhinosinusitis with nasal polyps. Auris Nasus Larynx. 2020 Jun;47(3):401-409.
51.Ryu G, Bae JS, Kim JH, Kim EH, Lyu L, Chung YJ, Mo JH. Role of IL-17A in Chronic Rhinosinusitis With Nasal Polyp. Allergy Asthma Immunol Res. 2020 May;12(3):507-522.
52.Peng Y, Ao M, Dong B, Jiang Y, Yu L, Chen Z, Hu C, Xu R. Anti-Inflammatory Effects of Curcumin in the Inflammatory Diseases: Status, Limitations and Countermeasures. Drug Des Devel Ther. 2021 Nov 2;15:4503-4525.
53.Madison R Smith, Lisa R Forbes Satter, Alexander Vargas-Hernández. STAT5b: A master regulator of key biological pathways. Front Immunol. 2023 Jan 23:13:1025373.
54.Robert Linke, Ralph Pries, Michael Könnecke, Karl Ludwig Bruchhage, Robert Böscke, Maximilian Gebhard, Barbara Wollenberg. Increased activation and differentiated localization of native and phosphorylated STAT3 in nasal polyps. Int Arch Allergy Immunol. 2013;162(4):290-8.
55.Linke R, Pries R, Könnecke M, Bruchhage KL, Böscke R, Gebhard M, Wollenberg B. Increased phosphorylation of STAT5b, but not STAT5a, in nasal polyps. Am J Rhinol Allergy. 2015 May-Jun;29(3):182-7.
56.Linke R, Pries R, Könnecke M, Bruchhage KL, Böscke R, Gebhard M, Wollenberg B. Increased activation and differentiated localization of native and phosphorylated STAT3 in nasal polyps. International archives of allergy and immunology. 2013 Oct 18;162(4):290-8.
57.Cheng AL, Hsu CH, Lin JK, Hsu MM, Ho YF, Shen TS, Ko JY, Lin JT, Lin BR, Ming-Shiang W, Yu HS, Jee SH, Chen GS, Chen TM, Chen CA, Lai MK, Pu YS, Pan MH, Wang YJ, Tsai CC, Hsieh CY. Phase I clinical trial of curcumin, a chemopreventive agent, in patients with high-risk or pre-malignant lesions. Anticancer Res. 2001;21:2895–2900.
58.Sharma RA, McLelland HR, Hill KA, Ireson CR, Euden SA, Manson MM, Pirmohamed M, Marnett LJ, Gescher AJ, Steward WP. Pharmacodynamic and pharmacokinetic study of oral Curcuma extract in patients with colorectal cancer. Clin Cancer Res. 2001;7:1894–1900.
59.Shoba, G., Joy, D., Joseph, T., Majeed, M. et al., Influence of piperine on the pharmacokinetics of curcumin in animals and human volunteers. Planta Med. 1998, 64, 353–356.
60.Schiborr C, Kocher A, Behnam D, Jandasek J, Toelstede S, Frank J. The oral bioavailability of curcumin from micronized powder and liquid micelles is significantly increased in healthy humans and differs between sexes. Mol Nutr Food Res. 2014 Mar;58(3):516-27. doi: 10.1002/mnfr.201300724. Epub 2014 Jan 9.
61.Junhu Tai, Jae-Min Shin, Jaehyung Park, Munsoo Han, Tae Hoon Kim. Oxidative Stress and Antioxidants in Chronic Rhinosinusitis with Nasal Polyps. Antioxidants (Basel). 2023 Jan 14;12(1):195.



